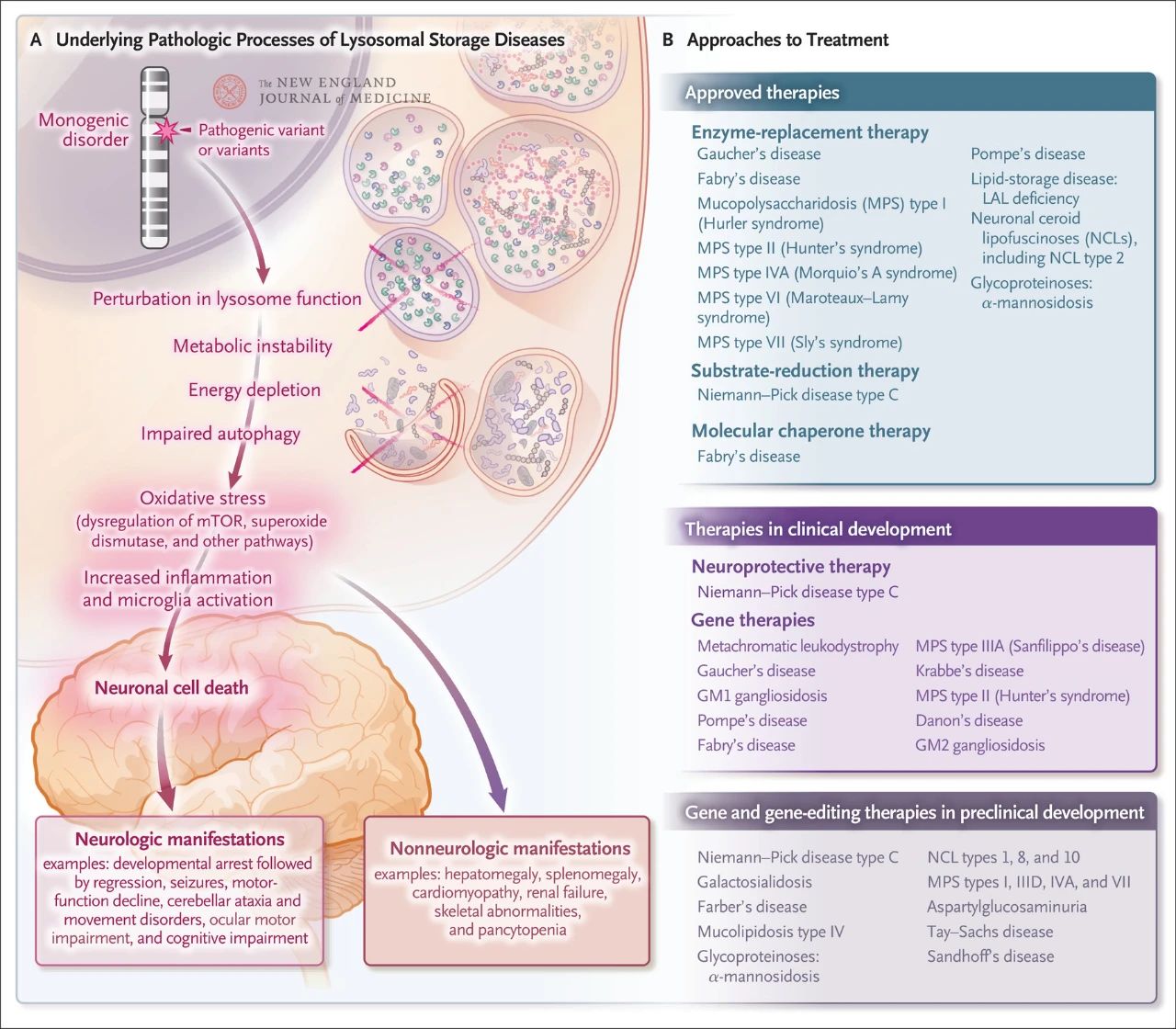
Иако релативно ретка, укупна инциденца лизозомског складиштења је око 1 на сваких 5.000 живорођених. Поред тога, од скоро 70 познатих поремећаја лизозомског складиштења, 70% погађа централни нервни систем. Ови поремећаји једног гена узрокују лизозомску дисфункцију, што резултира метаболичком нестабилношћу, дисрегулацијом циљног протеина рапамицина код сисара (mTOR, који нормално инхибира упалу), оштећеном аутофагијом и смрћу нервних ћелија. Неколико терапија усмерених на основне патолошке механизме лизозомске болести складиштења је одобрено или је у развоју, укључујући терапију замене ензима, терапију смањењем супстрата, терапију молекуларним шаперонима, генску терапију, уређивање гена и неуропротективну терапију.
Ниман-Пикова болест типа Ц је поремећај ћелијског транспорта холестерола у лизозомима узрокован биалелним мутацијама у NPC1 (95%) или NPC2 (5%). Симптоми Ниман-Пикове болести типа Ц укључују брзо, фатално неуролошко опадање у детињству, док касни јувенилни, јувенилни и одрасли облици укључују спленомегалију, супрануклеарну парализу погледа и церебеларну атаксију, дизартикулацију и прогресивну деменцију.
У овом броју часописа, Бремова-Ертл и сарадници извештавају о резултатима двоструко слепог, плацебо контролисаног, унакрсног испитивања. У испитивању је коришћен потенцијални неуропротективни агенс, аналог аминокиселине N-ацетил-L-леуцин (NALL), за лечење Ниман-Пикове болести типа C. Регрутовано је 60 симптоматских адолесцентних и одраслих пацијената, а резултати су показали значајно побољшање укупног резултата (примарни крајњи циљ) на скали за процену и оцењивање атаксије.
Клиничка испитивања N-ацетил-DL-леуцина (Танганил), рацемске супстанце NALL и n-ацетил-D-леуцина, изгледа да су углавном вођена искуством: механизам деловања није јасно разјашњен. N-ацетил-DL-леуцин је одобрен за лечење акутне вртоглавице од 1950-их; животињски модели сугеришу да лек делује тако што ребалансира прекомерну поларизацију и деполаризацију медијалних вестибуларних неурона. Након тога, Струп и др. су објавили резултате краткорочне студије у којој су приметили побољшања симптома код 13 пацијената са дегенеративном церебеларном атаксијом различитих етиологија, налази који су поново покренули интересовање за поновно испитивање лека.
Механизам којим н-ацетил-ДЛ-леуцин побољшава функцију нерава још увек није јасан, али налази на два модела мишева, једном са Ниман-Пиковим обољењем типа Ц и другом са поремећајем складиштења ганглиозида ГМ2 варијанте О (Сандхофова болест), још једном неуродегенеративном лизозомском болешћу, подстакли су пажњу да се усмери на НАЛЛ. Конкретно, преживљавање Нпц1-/- мишева третираних н-ацетил-ДЛ-леуцином или НАЛЛ-ом (Л-енантиомери) се побољшало, док преживљавање мишева третираних н-ацетил-Д-леуцином (Д-енантиомери) није, што сугерише да је НАЛЛ активни облик лека. У сличној студији поремећаја складиштења ганглиозида ГМ2 варијанте О (Хексб-/-), н-ацетил-ДЛ-леуцин је резултирао скромним, али значајним продужењем животног века код мишева.
Да би истражили механизам деловања н-ацетил-ДЛ-леуцина, истраживачи су истраживали метаболички пут леуцина мерењем метаболита у ткивима малог мозга мутираних животиња. У варијанти О модела поремећаја складиштења ганглиозида ГМ2, н-ацетил-ДЛ-леуцин нормализује метаболизам глукозе и глутамата, повећава аутофагију и повећава нивое супероксид дисмутазе (активног хватача кисеоника). У Ц моделу Ниман-Пикове болести, примећене су промене у метаболизму глукозе и антиоксиданата и побољшања у метаболизму митохондријалне енергије. Иако је Л-леуцин снажан активатор mTOR-а, није било промене у нивоу или фосфорилацији mTOR-а након третмана са н-ацетил-ДЛ-леуцином или његовим енантиомерима ни у једном моделу на мишу.
Неуропротективни ефекат NALL-а је примећен код мишевог модела повреде мозга изазване кортикалним импингментом. Ови ефекти укључују снижавање неуроинфламаторних маркера, смањење смрти кортикалних ћелија и побољшање аутофагијског флукса. Након третмана NALL-ом, моторичке и когнитивне функције повређених мишева су обновљене, а величина лезије је смањена.
Инфламаторни одговор централног нервног система је обележје већине неуродегенеративних поремећаја лизозомског складиштења. Ако се неуроинфламација може смањити лечењем NALL-а, клинички симптоми многих, ако не и свих, неуродегенеративних поремећаја лизозомског складиштења могу се побољшати. Као што ова студија показује, очекује се да ће NALL имати синергију са другим терапијама за болест лизозомског складиштења.
Многи поремећаји складиштења лизозома су такође повезани са церебеларном атаксијом. Према међународној студији која је обухватила децу и одрасле са поремећајима складиштења ганглиозида GM2 (Теј-Саксова болест и Сандхофова болест), атаксија је смањена, а координација фине моторике побољшана након лечења НАЛЛ-ом. Међутим, велико, мултицентрично, двоструко слепо, рандомизовано, плацебо контролисано испитивање показало је да н-ацетил-ДЛ-леуцин није био клинички ефикасан код пацијената са мешовитом (наслеђеном, ненаслеђеном и необјашњивом) церебеларном атаксијом. Ово откриће сугерише да се ефикасност може приметити само у испитивањима која укључују пацијенте са наслеђеном церебеларном атаксијом и анализираним повезаним механизмима деловања. Поред тога, пошто НАЛЛ смањује неуроинфламацију, која може довести до трауматске повреде мозга, могу се размотрити испитивања НАЛЛ-а за лечење трауматске повреде мозга.
Време објаве: 02.03.2024.